

前言
液相色谱-串联质谱法(LC-MS/MS)是临床生化小分子检测的首选方法,常用于血清25-羟维生素D[25(OH)D]的检测。其虽有高灵敏度、高特异性、线性范围宽等优势,但因仪器、色谱柱、试剂、校准物、方法学及性能验证等因素的影响,也会造成同一个实验室内部及不同实验室之间的LC-MS/MS检测结果存在较大偏差。标准化是确保在不同实验室、不同质谱仪器及不同时间,获得一致性和可比性结果的必要条件。为规范LC-MS/MS检测25(OH)D的方法,该共识基于目前现有的临床质谱相关指导文件和临床实践,针对同位素稀释LC-MS/MS的标准物质和内标物选择、方法验证、色谱质谱参数选择、质量控制、人员要求及参考区间等方面提出建议,旨在提高检验结果的准确性及可靠性。
文章摘选
维生素 D 与人体骨骼发育、自身免疫力、心血管健康等方面息息相关,维生素 D 缺乏、代谢异常或过量均会对健康产生较大影响,因此检验结果的 准确性对于临床评估机体基础水平、制定干预方案 等方面至关重要。目前血清维生素 D 检测方法主要为化学发光免疫分析法(chemiluminescent immunoassay,CLIA)和液相色谱‐串联质谱法(liquid chromatography‐ tandem mass spectrometry,LC‐MS/MS)。从检测原理出发,LC‐MS/MS 是基于被测生物标志物本身分子量、结构等化学性质的直接分析法,因此具有独 特高灵敏度、高特异性和高通量特点。CLIA是基于抗原抗体反应,与LC‐MS/MS相较,前处理简单且检测自动化程度高,但存在特异性低、线性范围窄和检测结果可比性差等问题。LC‐MS/MS首次运用于常规临床实验室时,其结果通常被认为准确可靠。然而目前LC‐MS/MS检 测25‐羟维生素D[25(OH)D]的方法大多为实验室自建方法,虽然已有多类质谱检测试剂盒陆续上 市,但方法缺乏标准化,无法避免因受仪器、色谱柱、试剂、校准物、方法性能验证等因素而导致检测结果差异很大。另外,方法验证指南的不适当解读和应用、标准物质的缺乏或不适当使用、质量保证措施的不完整均可导致检测结果的偏差甚至错误。LC‐MS/MS 检测血清 25(OH)D方法的标准化是其在临床实验室成功应用的必要条件,也是保证方法之间一致性和可比性的核心要素。本标准化涉及量值溯源、检测的特异度和精密度以及样本的前处理等过程,其中量值溯源可确保常规实验室检测结果溯源至国内或国际公认的参考测量系统, 保证检测结果的准确性。其检测特异性能避免血 清中的其他物质和基质的干扰,而好的精密度是保证实验室检测稳定性和重现性的必要条件。实验室目前可获得技术指导文件包括CLSI‐C62A 、《液相色谱‐质谱临床应用建议》 、《液相色谱串联质谱 临床检测方法的开发与验证》等。基于此,本专家共识旨在建立标准化的血清 25(OH)D 检测方法,从标准物质和内标物的选择、仪器与试剂的准备、检测方法注意事项、质量控制管理、人员要求及参考区间等方面提出建议。
术语与定义
1. 25(OH)D:人体血液中维生素D的主要循环形式包括25(OH)D2和25(OH)D3,其中25(OH)D3为 主要存在形式,因其稳定性好,可作为评价人体维生素D水平的可靠指标。2. 内标:加入到待测样品中,作为测定待测组分含量的参照标准及其已知质量或含量纯物质。3. 标准物质:具有足够均匀且稳定的特定特性物质,其特性适用于测量及标称特性检查的用途。4. 有证标准物质:附有由权威机构发布文件, 提供使用有效程序获得且具有不确定度和溯源性的一个或多个特性值标准物质。5. 定量下限(limit of quantitation,LOQ):在规定的测量条件下,以指定的测量不确定度能测量的样品中可被测量的最低值。
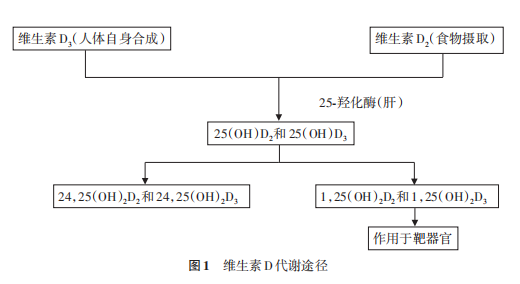
维生素D主要生理功能及代谢路径
维生素D主要生理功能及代谢路径人体维生素D缺乏、代谢异常或过量均会影响肠道钙、磷吸收和骨代谢。此外,维生素D与心血管细胞上的维生素D受体结合,低水平状态时, 机体可通过激活促炎症瀑布导致内皮功能异常和动脉壁的硬度增加而加重心血管疾病的危险性。维生素 D受体亦存在于免疫系统的细胞中,通过与受体结合可降低细胞因子(炎症蛋白质)水平,并且增加抗菌肽的含量,已有研究表明,充足的维生素D水平可预防呼吸道感染。由于维生素D是一种脂溶性维生素,易储存于体内(主要肝脏),过量时可产生不良反应。因此,精准的检测结果可帮助临床准确评估人体维生素D营养状态、吸收障碍或毒性水平。人体维生素D主要来源于皮肤经阳光作用合成的维生素 D3,另一种来源是食物中(如经光照后的蘑菇、野生海鱼等)的维生素D2,两者通过肝脏代谢后以 2 种形式存在 ,分别是 25(OH)D2 和 25(OH)D3,虽然人体血液中超过 95% 的 25(OH)D为 25(OH)D3,但仍存在少量 25(OH)D2,若补充外源性 25(OH)D2,则体内可检测出浓度较高的 25(OH)D2,因此需分别对25(OH)D2和25(OH)D3进行定量检测。25(OH)D在肾脏和其他组织中转变 为具有生物活性的二羟基代谢物1,25‐羟基维生素 D[1,25(‐ OH)2D],该物质经过维生素D结合蛋白转运至靶器官,与维生素D受体结合,从而发挥其生理作用(图1)。1,25(‐ OH)2D在人体内的浓度低 (pg/ml级别)、半衰期短,检测难度较大,而25(OH)D因其浓度高、稳定、半衰期较长,是反映机体维生素D代谢的重要检测指标。此外,25(OH)D3 与3‐epi‐25‐羟基维生素D3[3‐epi‐25(OH)D3]为同分异构体,其质荷比一致而导致无法通过质谱直接分离,一般可通过色谱分离的方式使这2种分析物具有不同保留时间;当分离度达到1.5时,可忽略3‐epi‐25(OH)D3对 25(OH)D3检测的影响。在学龄儿童体内,3‐epi‐25(OH)D3占 25(OH)D 的2.5%~ 17%,但在出生后前3个月婴儿体内,3‐epi‐25(OH)D3 浓度较高 ,占 25(OH)D 浓度的60%,在成人中占比较低,偶尔可高达 22%。
LC‐MS/MS技术
LC‐MS/MS是通过质量分析器测定带电粒子质 荷比的一种分析技术;MS/MS是将 2个质量分析器由碰撞室串接起来的分析设备,即三重四极杆质谱仪。第一级质量分析器筛选出被离子化的样本中 特定质荷比的母离子,母离子进入碰撞室,通过碰撞诱导解离的方式形成碎片子离子;第二级质量分析器筛选出特异性强的定量子离子及定性子离子, 子离子进入检测器监测,最终得到目标分析物的含量。每个母离子/子离子对被称为1个离子对,只有具有特定离子对的待测物质,才能进入检测器。因此,MS/MS具有很好的检测特异性。此外,质谱方法具有同时监测多离子通道多反应监测 (multiple reaction monitoring, MRM)的独特优势,即使在检测背景信号高的内源性化合物时,亦可通过同时监测 2 个离子碎片通道, 实现待测物质的精准检测。
参考文献:[1]中国老年保健医学研究会检验医学分会, 中国老年医学学会检验医学分会. 液相色谱-串联质谱法检测25-羟维生素D标准化专家共识[J]. 中华检验医学杂志 2021年44卷7期, 587-595页, ISTIC PKU CSCD CA, 2021.